Università degli Studi di Napoli Federico II
Oleochimica: utilizzo di materie prime rinnovabili
Metodi analitici utilizzati per oli vegetali e prodotti di transesterificazione (biodisel)
A.1 Analisi spettroscopica 1H-NMR
La spettroscopia NMR si è rivelata un'ottima tecnica per la determinazione diretta degli esteri metilici presenti nei prodotti di transesterificazione e per la valutazione della resa di reazione.
Vengono riportati di seguito gli spettri relativi all'olio di partenza, in questo caso olio di semi di soia, alla fase esterea prodotta da una reazione di transesterificazione con bassi valori di conversione e a quella prodotta dopo una reazione giunta a conversione totale.
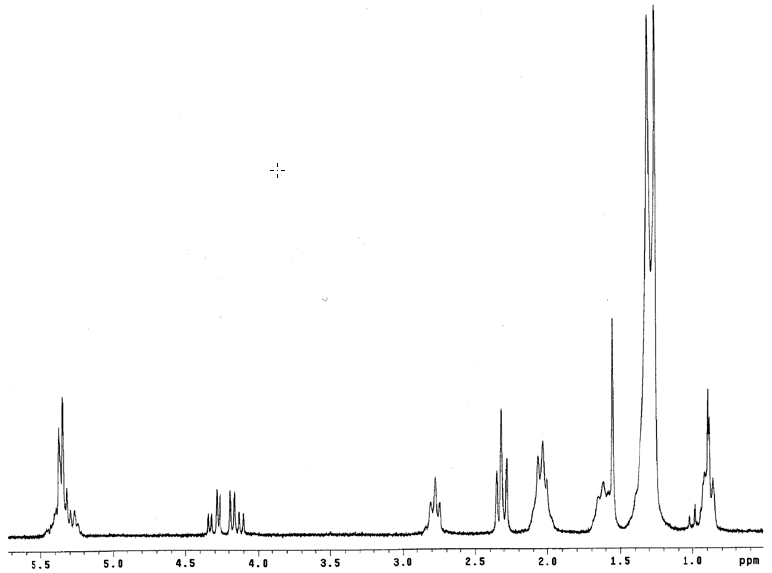 |
| Figura A.1 - Spettro 1H-NMR dell'olio di semi di soia. |
I segnali fondamentali per seguire l'avanzamento della reazione sono quelli caratteristici del gruppo metossilico (che appare come singoletto a 3.7 ppm) e del gruppo metilenico in α al gruppo carbonilico (esso è presente indipendentemente dalla resa della reazione ed appare come tripletto in corrispondenza del chemical shift di 2.3 ppm).
Altri segnali, che è possibile distinguere osservando ciascuno spettro sono quelli del gruppo glicerico intorno a 4.2 ppm, del gruppo vinilico (−CH=CH2) a 5.3 ppm e del gruppo allilico (−CH2−CH=CH2) a 2.1 ppm.
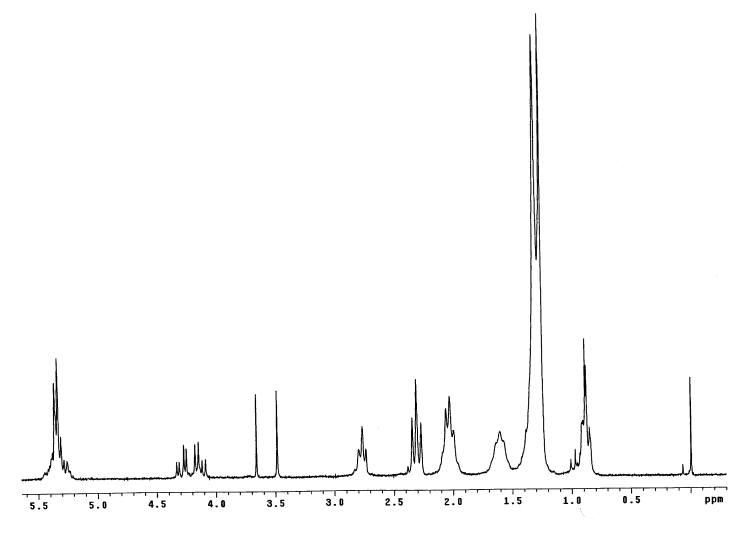 |
| Figura A.2 - Spettro 1H-NMR degli esteri prodotti da una reazione di transesterificazione con bassi valori di conversione. |
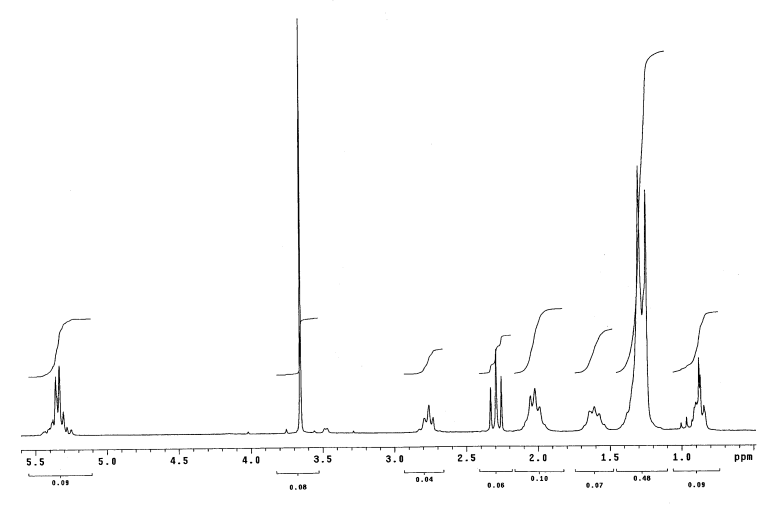 |
| Figura A.3 - Spettro 1H-NMR degli esteri prodotti da una reazione di transesterificazione giunta a conversione totale. |
Dal confronto diretto tra questi tre spettri, si può notare come il fattore determinante nel calcolo della resa della reazione di transesterificazione sia il segnale relativo ai gruppi metossilici; questo, infatti, compare solo dopo l'avanzamento della reazione e in misura proporzionale alla conversione raggiunta, mentre i gruppi metilenici sono sempre presenti, sia nell'olio di partenza, che nei prodotti di reazione nelle stesse quantità.
Data la formula chimica del generico estere:
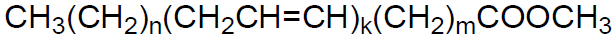 |
ESTERE METILICO |
se si indica con A1 l'area d'integrazione del segnale relativo al gruppo metossile (che compare a 3.7 ppm):
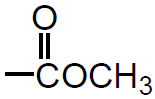 |
GRUPPO METOSSILE |
e con A2 l'area d'integrazione del segnale relativo al gruppo metilenico in α al gruppo carbonilico (con chemical shift di 2.3ppm):
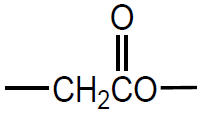 |
GRUPPO METILENICO |
la resa di reazione, espressa in termini di conversione dei trigliceridi, può essere calcolata direttamente dalla combinazione delle aree, ottenute dall'integrazione dei picchi sopra menzionati, moltiplicato un fattore di correzione che tiene conto del numero di protoni interessati:
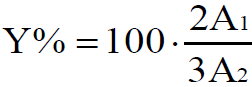
A.2 Analisi Gascromatografica
- Il metodo
Il metodo descrive un procedimento per la determinazione simultanea del contenuto di glicerina libera, monogliceridi, digliceridi, trigliceridi e metilesteri presenti nel biodiesel mediante analisi gascromatografica.
La trimetilsililazione di glicerina, monogliceridi e digliceridi seguita da una separazione gascromatografica mediante una colonna capillare con fase stazionaria di bassa polarità permette la determinazione quantitativa degli analiti mediante un'unica corsa gascromatografica. - Principio del metodo
Il biodiesel è costituito da metilesteri ottenuti mediante transesterificazione con metanolo di oli vegetali o grassi animali; la presenza di quantità significative di glicerina, monogliceridi, digliceridi e trigliceridi è dovuta ad una transesterificazione incompleta o alla insufficiente purificazione del biodiesel stesso. Esistono, tuttavia, dei limiti alle quantità permesse di glicerina, mono-, di- e trigliceridi presenti nel biodiesel.
Il metodo descrive una procedura gascromatografica che impiega una colonna capillare con fase stazionaria apolare per la determinazione simultanea e quantitativa di glicerina libera, mono-, di- e trigliceridi.
Prima di eseguire l'analisi gascromatografica occorre derivatizzare i campioni, ossia variare considerevolmente la volatilità e la polarità dei componenti presenti. La derivatizzazione consiste nella trimetilsililazione dei gruppi idrossilici liberi di glicerina, monogliceridi e digliceridi.
L'uso di due standard interni, metileptadecanoato e 1,2,4-butantriolo, permette la determinazione quantitativa di metilesteri, mono-, di-, trigliceridi e glicerina libera mediante il calcolo dei relativi fattori di risposta.
Il calcolo dei fattori di risposta viene eseguito analizzando una soluzione standard contenente glicerina, una monooleina, una dioleina, una trioleina e i due standard interni. - Apparecchiatura
3.1 - Gascromatografo Clarus 500 della Perkin Elmer equipaggiato con iniettore on-column e rivelatore a ionizzazione di fiamma.
3.2 - Colonna gascromatografica capillare in silice fusa con fase stazionaria 5% fenil 95% dimetilpolisilossano (DB-5, HP-5, SE52, etc.):- lunghezza: 10m
- diametro interno: 0.32 mm
- spessore: 0.1 μm
3.4 - Microsiringhe da 1 μl con ago per iniezione on-column
3.5 - Provette graduate munite di tappo
3.6 - Pipette Pasteur
3.7 - Bombola di azoto
3.8 - Micropipette Gilson 100:1000
3.9 - Matracci da 10, 50 e 100 ml
3.10 - Bilancia analitica con precisione ± 0.0001 - Reagenti
4.1 - Eptano di grado analitico
4.2 - Esano di grado analitico
4.3 - Piridina di grado analitico
4.4 - Glicerina (>99%)
4.5 - (S)-(-)-1,2,4-butantriolo (standard interno)
4.6 - 1-mono[cis-9-octadecenoil]-rac-glicerolo (monooleina)
4.7 - 1,3-di-[cis-9-octadeceniol]glicerolo (dioleina 4.8 - 1,2,3-tri-[cis-9-octadeceniol]glicerolo (trioleina)
4.9 - Metileptadecanoato (>99%) (standard interno)
4.10 - N,O-bis(trimetilsilil)trifluoruroacetammide + 1% trimetilclorosilano (BSFTA + 1% TMCS) - Procedimento
5.1 - Preparazione delle soluzioni standard per il calcolo dei fattori di risposta
5.1.1 - Preparazione della soluzione standard di metileptadecanoato: in un matraccio da 100 ml pesare 0.1 g di standard e portare a volume con esano (concentrazione effettiva = 1 mg/ml)
5.1.2 - Preparazione della soluzione standard di 1,2,4-butantriolo: in un matraccio da 100 ml pesare 0.1 g di standard e portare a volume con piridina (concentrazione effettiva = 1mg/ml)
5.1.3 - Preparazione della soluzione standard di glicerina: in un matraccio da 10 ml pesare 10 mg di standard e portare a volume con piridina (concentrazione effettiva = 1.86 mg/ml)
5.1.4 - Preparazione della soluzione standard di monooleina: in un matraccio da 10 ml pesare 10 mg di standard e portare a volume con piridina (concentrazione effettiva = 1 mg/ml)
5.1.5 - Preparazione della soluzione standard di dioleina: in un matraccio da 10 ml pesare 10 mg di standard e portare a volume con piridina (concentrazione effettiva = 1 mg/ml)
5.1.6 - Preparazione della soluzione standard di trioleina: in un matraccio da 100 ml pesare 500 mg di standard e portare a volume con piridina (concentrazione effettiva = 4.09 mg/ml)
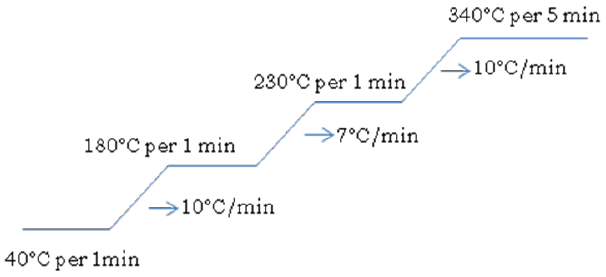
5.2 - Scelta delle condizioni operative:- pressione in colonna: 10 psia
- programma di temperatura
- Iniettore on-column spento
- Temperatura del rivelatore (FID):350°C
5.3 - Preparazione dello standard per il calcolo dei fattori di risposta.
Introdurre in una provetta graduata con tappo a vite 1 ml della soluzione standard di metileptadecanoato (5.1.1), 1 ml della soluzione standard di 1,2,4-butantriolo (5.1.2), 1 ml della soluzione standard di glicerina (5.1.3), 1 ml della soluzione standard di monooleina (5.1.4), 1 ml della soluzione standard di dioleina (5.1.5) e 1 ml della soluzione standard di trioleina (5.1.6). Si lascia evaporare il solvente sotto il flusso di azoto. Realizzare l'operazione a temperatura ambiente evitando riscaldamenti del campione.
Addizionare al campione, completamente privato dei solventi, 300μl di BSFTA + 1% TMCS e 300 μl di piridina. Tappare la provetta e lasciare a temperatura ambiente per 20 minuti circa. Al termine della reazione evaporare la piridina e l'agente silanilizzante sotto flusso di azoto senza riscaldare.
Ad evaporazione completata aggiungere immediatamente 8 ml di eptano e tappare la provetta. Conservare la provetta in assenza di umidità.
5.4 - Preparazione del campione
In un matraccio da 50 ml pesare 0.5 ± 0.0001 g di biodiesel e portare a volume con esano. Tappare il contenitore ed agitare. Trasferire 1 ml della soluzione del campione mediante pipetta a bolla in una provetta a fondo conico. Aggiungere 1 ml della soluzione standard di metileptadecanoato (5.1.1). Trattare con flusso di azoto per allontanare il solvente. Realizzare l'operazione a temperatura ambiente evitando riscaldamenti del campione. Addizionare al campione, completamente privato del solvente, 300μl di BSFTA + 1% TMCS e 300μl di piridina. Tappare la provetta e lasciare a temperatura ambiente per 20 minuti circa. Al termine della reazione evaporare la piridina e l'agente silanilizzante sotto flusso di azoto senza riscaldare. Ad evaporazione completata aggiungere immediatamente 8 ml di eptano e tappare la provetta. Conservare la provetta in assenza di umidità.
5.5 - Esecuzione delle analisi
Si preleva 1μl della soluzione del campione con la micro siringa, si aspira aria e si asciuga l'estremità dell'ago. Si introduce l'ago attraverso la membrana sul portello dell'iniettore on-column seguendo l'introduzione dell'ago (flessibilissimo) con l'aiuto delle dita, si preme lo stantuffo rapidamente fino in fondo e dopo 5-7 secondi si estrae l'ago.
Nel cromatogramma l'ordine di eluizione sarà il seguente: glicerina libera, metilesteri, monogliceridi, digliceridi, trigliceridi. - - Valutazione quantitativa ed espressione dei
risultati
6.1 - Calcolo dei fattori di risposta
Si inietta al gascromatografo 1 μl dello standard preparato come al punto 5.3. Si procede al calcolo delle aree di ogni singolo picco mediante integrazione dal computer. Prendendo come riferimento il metileptadecanoato e assegnando 1 al fattore di risposta del metileptadecanoato, si ricavano gli altri fattori di risposta come segue:fattore monogliceridi = (Amono · Cmet) / (Amet · Cmono)
Esprimendo i risultati con due cifre decimali si ottiene:
fattore digliceridi = (Adi · Cmet) / (Amet · Cdi)
fattore trigliceridi = (Atri · Cmet) / (Amet · Ctri)
fattore glicerina = (Agly · Cbut) / (Abut · Cgly)
in cui:
Amono = area del picco della monooleina
Adi = area del picco della dioleina
Atri = area del picco della trioleina
Agly = area del picco della glicerina
Amet = area del picco del metileptadecanoato
Abut = area del picco del 1,2,4-butantriolo
Cmono = concentrazione della soluzione standard di monooleina (1 mg/ml)
Cdi = concentrazione della soluzione standard di dioleina (1 mg/ml)
Ctri = concentrazione della soluzione standard di trioleina (4.09 mg/ml)
Cbut = concentrazione della soluzione standard di 1,2,4-butantriolo (1 mg/ml)
Cgly = concentrazione della soluzione standard di glicerina (1.86 mg/ml)fmet = 1
6.2 – Calcolo della % in peso di metilesteri, mono-, di-, trigliceridi e glicerina libera
fmono = 1.77
fdi = 0.7
ftri = 0.5
fgly = 1.18
Si inietta al gascromatografo 1μl del campione preparato come al punto 5.4. Si procede al calcolo delle aree di ogni singolo picco mediante integratore elettronico. Dal cromatogramma si ricavano le sommatorie delle aree dei metilesteri, dei monogliceridi, dei digliceridi, dei trigliceridi e l'area del picco della glicerina libera.
Si procede al calcolo percentuale come segue:mgmet = (Smet · Cmet) / (Amet · fmet)
I valori ottenuti sono normalizzati al 99% poiché bisogna considerare l'1% di sostanze non gliceridiche (steroli, idrocarburi, cere, etc.) comunque presenti negli oli di partenza.
mgmono = (Smono · Cmet) / (Amet · fmono)
mgdi = (Sdi · Cmet) / (Amet · fdi)
mgtri = (Stri · Cmet) / (Amet · ftri)
mggly = (Agly · Cbut) / (Abut · fgly)
St = mgmet + mgmono + mgdi + mgtri + mggly
% metilesteri = (mgmet · 99) / St
% monogliceridi = (mgmono · 99) / St
% digliceridi = (mgdi · 99) / St
% trigliceridi = (mgtri · 99) / St
% glicerina = (mggly · 99) / St
Esprimere i risultati con una cifra decimale.Dove:
Di seguito si riporta un cromatogramma ottenuto con il Clarus 500 per degli esteri prodotti da una reazione di transesterificazione con elevati valori di conversione.
Smet = sommatoria delle aree dei metilesteri
Smono = sommatoria delle aree dei monogliceridi
Sdi = sommatoria delle aree dei digliceridi
Stri = sommatoria delle aree dei trigliceridi
Amet = area del picco del metileptadecanoato
Abut = area del picco dell'1,2,4-butantriolo
Cmet = concentrazione della soluzione standard di metileptadecanoato
Fmono = fattore di risposta dei monogliceridi
Fdi = fattore di risposta dei digliceridi
Ftri = fattore di risposta dei trigliceridi
Fgly = fattore di risposta della glicerina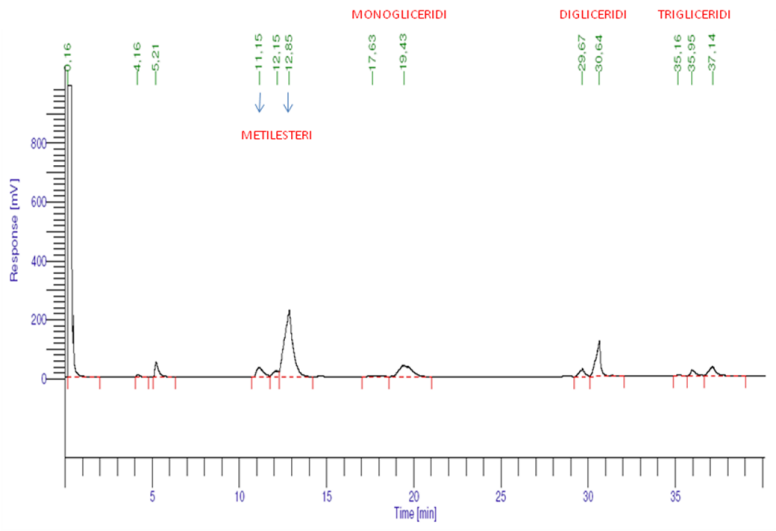
Figura A.4 - Cromatogramma degli esteri prodotti da una reazione di transesterificazione con elevati valori di conversione.
L'acidità di un olio viene generalmente espressa in termini di percentuale in peso di acido oleico contenuto nel substrato. Questo valore viene determinato seguendo la procedura di titolazione indicata dal metodo NGD C 10 (1976).
La soluzione titolante è una soluzione di idrossido di sodio 0,1 N.
Tale titolazione richiede una massa di sostanza grassa che va dai 3 ai 20 grammi; questa massa viene disciolta in 100 ml della miscela etanolo-etere etilico, in rapporto volumetrico 1:2, contenente poche gocce di indicatore fenolftaleina e successivamente titolata con la soluzione di idrossido di sodio fino al viraggio.
Il valore dell'acidità viene calcolato in questo modo:
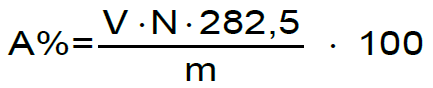
V= volume della soluzione titolante, NaOH, consumato, espresso in litri;L'acidità di una sostanza grassa viene comunemente espressa anche come "numero di acidità", definito come milligrammi di idrossido di potassio necessari per neutralizzare un grammo di sostanza grassa. Questo valore viene determinato seguendo la procedura di titolazione indicata dal metodo ASTM D 4662-03.
N= normalità della soluzione titolante;
m= massa del campione prelevato per l'analisi, espressa in grammi;
282,5= peso molecolare dell'acido oleico, espresso in grammi/mol.
Questo metodo misura l'acidità dei polioli, dove a determinare l'acidità sono più composti acidi diversi o di cui non si è a conoscenza della formula chimica, e di altri materiali di alta acidità che sono solubili in miscele di toluene ed alcol etilico, usati come solventi.
In tal caso il valore dell'acidità sarŕ così individuato:
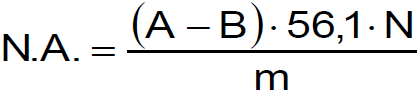
Dove
A= soluzione di KOH per titolare il campione, mL
B= soluzione di KOH per titolare il bianco (solo solvente), mL
56,1= peso molecolare di KOH
A.4 Analisi gas-cromatografica della composizione di un trigliceride
A seconda della provenienza del grasso la composizione dei trigliceridi è molto variabile. Di conseguenza la determinazione della composizione acidica in campioni di olio, burro, margarina, ed in prodotti contenenti frazioni significative di sostanza grassa (alimenti, cosmetici, farmaci, ecc.) risulta essenziale per una loro caratterizzazione sia in termini di composizione che di qualità del prodotto.
L'analisi degli acidi grassi può essere convenientemente eseguita per via gas-cromatografica, sfruttando la volatilità dei loro esteri metilici che è maggiore sia degli acidi grassi liberi che dei trigliceridi originali.
La composizione qualitativa degli acidi grassi presenti nel campione si fa per confronto con una miscela standard a composizione nota di esteri metilici degli acidi grassi; oppure, sulla base delle proprietà della fase stazionaria, si può prevedere il seguente ordine di eluizione:
- il tempo di ritenzione aumenta all'aumentare del numero di atomi di carbonio;
- gli esteri insaturi eluiscono dopo i corrispondenti esteri saturi;
- il tempo di ritenzione degli esteri insaturi aumenta all'aumentare del numero di doppi legami;
- gli esteri ramificati escono prima degli esteri lineari con uguale numero di atomi di carbonio;
L'analisi quantitativa si basa sulla misura dell'area di ogni picco (in pratica di tutti tranne quelli attribuibili al solvente), esprimendo ogni concentrazione come area relativa (% w/w), nell'ipotesi che tutti i componenti vengano eluiti (cioè se la corsa è sufficientemente lunga).
Sarebbe possibile ottenere dei valori percentuali più accurati calcolando i fattori di risposta dei singoli esteri metilici degli acidi grassi. Ciò si potrebbe fare preparando ed analizzando una miscela a contenuto noto di ogni estere. I fattori di risposta si otterrebbero prendendo uno degli analiti come riferimento (fi = 1), oppure utilizzando uno standard interno.
E' riportata una procedura standard per l'analisi di un olio
Reagenti
- acido solforico al 98%
- metanolo
- n-esano
- standard singoli o in miscela dei principali esteri metilici degli acidi grassi
- carbonato di sodio
- solfato di sodio anidro (oppure solfato di magnesio anidro)
- gas-cromatografo equipaggiato con colonna capillare polare, per esempio EC-WAX (30 m) e rivelatore FID
- integratore o computer
- bagno riscaldante
- fiala da 20 mL munita di setto rivestito in teflon e ghiera in allumino (con cup crimper)
- pipetta graduata da 1 mL
- pipetta tarata da 2 mL
- pipetta tarata da 5 mL
- pipetta Pasteur con tettarella
- siringa da GC da 5 μL
- spatolina in acciaio
- 6 matracci da 2 o 5 mL
Preliminarmente è necessario metilare i campioni di lipide, quindi si procede all'analisi sul gas-cromatografo opportunamente impostato.
- Introdurre nella fiala circa 0.5 g di campione di olio;
- Aggiungere 2 mL di metanolo e 80 μL di acido solforico concentrato (98%) utilizzando una pipetta graduata da 1.0 mL. Att. Seguire questo ordine di aggiunta dei reagenti. L'acido solforico va introdotto con cautela perché la sua solvatazione è fortemente esotermica.
- Chiudere con setto e ghiera la fiala;
- Indossando occhiali protettivi porre la fiala in un bagno termostatico alla temperatura di 80 °C per 40 minuti;
- Nel frattempo preparare una soluzione sciogliendo la minima quantità possibile per ogni estere metilico a disposizione in n-esano, e successivamente una soluzione contenente una miscela di questi, utilizzando dei matracci da 2 o 5 mL od una fiala con tappo, di volume opportuno; se invece è disponibile una miscela standard commerciale, diluirla opportunamente prima di iniettarla;
- Raffreddare la fiala a temperatura ambiente con acqua corrente, dopo aver tolto il sostegno metallico;
- Aprire la fiala e introdurre 5 mL di n-esano;
- Agitare bene in modo da estrarre completamente gli esteri metilici nella fase organica (strato superiore) e poi separare la fase organica (per esempio con una Pasteur) e conservarla a parte; se la soluzione è appena torbida (per la presenza di acido solforico), aggiungere del carbonato di sodio e agitare fino al termine dell'effervescenza; aggiungere poi del solfato di sodio o di magnesio anidro per eliminare l'acqua residua;
- Impostare l'apparecchio: una colonna cromatografica adatta è una EC-WAX. Si imposta il metodo di analisi (tra cui i valori di T iniettore, T rivelatore, T colonna; i valori normalmente impiegati con una colonna EC-WAX sono: T iniettore = 230 – 250 °C, T rivelatore = 260 °C, T colonna = 180 – 200 °C). Si regola il flusso del gas di trasporto (per es. 14 psi (se necessario). Si selezionano i parametri di acquisizione ed integrazione del segnale;
- Iniettare i singoli standard, 0.3 μL, e poi la miscela di questi, verificando la sequenza di uscita;
- Se tutti i picchi risultano separati procedere col campione, altrimenti modificare le condizioni di separazione (T della colonna od eventuale rampa di temperatura);
- Iniettare 0.3 μL di campione (fase organica) nel gas-cromatografo nelle condizioni scelte, 2 o 3 volte.
Riportare nella relazione un cromatogramma della miscela degli standard ed un cromatogramma del campione.
